 이미지 확대보기
이미지 확대보기4일 뉴욕증시 따르면 나스닥거래소에서 길리어드 사이언스 주가는 지난 주말 79.75달러로 마감했다. 전일대비 4.05달러, 비율로는 무려 4.82% 떨어진 것이다.
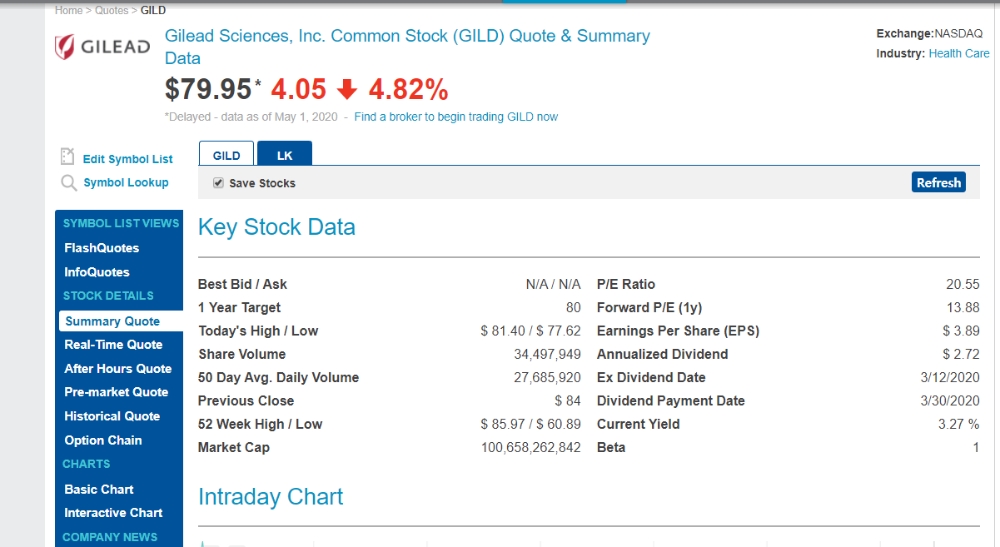
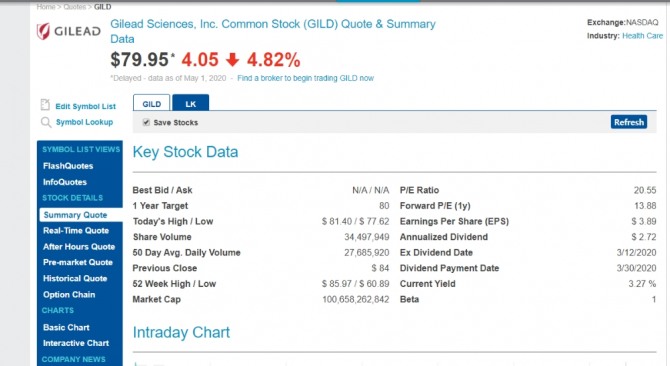
다음은 FDA 렘데시비르 긴급 승인 직후인 주말 길리어드 사이언스(Gilead) 마감 주가
Key Stock Data Best Bid / AskN/A / N/A
1 Year Target80 Today's High / Low$ 81.40 / $ 77.62
Share Volume34,497,949
50 Day Avg. Daily Volume27,685,920
Previous Close$ 84
52 Week High / Low$ 85.97 / $ 60.89
Market Cap100,658,262,842
Forward P/E (1y)13.88
Earnings Per Share (EPS)$ 3.89
Annualized Dividend$ 2.72
Ex Dividend Date3/12/2020
Dividend Payment Date3/30/2020
Current Yield3.27 %
Beta 1
권준욱 중앙방역대책본부 부본부장은 지난 주말 정례브리핑에서 "렘데시비르의 특례수입절차를 빠르게 진행하는 방안에 대해 충분히 대비하고 진행하고 있다"고 말했다. 약사법상의 특례수입조항에 해당하면 국내 품목 허가나 신고가 되지 않은 의약품도 제조·수입이 가능하다.
미국 식품의약국(FDA)은 지난 주말 렘데시비르는 길리어드사이언스(이하 길리어드)가 에볼라 치료제로 개발해온 항바이러스제로, 최근 미국에서 진행한 초기 임상시험에서 코로나19 치료에 효과가 나타났다고 ㅂ보고 렘데시비르에 대한 긴급사용을 승인했다.
권 부본부장은 이완관련 "미국 FDA 긴급사용 승인은 정식 사용 승인은 아니다"고 언급하면서 며 코로나19가 의심되거나 확진된 환자 중 중증인 환자의 치료에 국한해 사용할 수 있게 된 것이라고 설명했다. 그러면서 임상시험 결과를 더 지켜봐야 한다고 강조했다. 렘데시비르 관련 임상시험은 전 세계에서 계속 진행 중이다. 우리나라에서도 3건의 임상시험이 진행되고 있다.
권 준욱 부본부장은 "방역 당국으로서 관계 당국·부처와 긴밀히 협조하고 전문가들과 논의하면서 렘데시비르 임상 시험 결과를 정리하겠다"고 밝혔다. 그는특히 "임상시험 결과는 전문가들의 영역이다. 일부는 통계학적인 유의성에 의문을 표시하는 전문가들도 있다"면서도 "그런데도 현재 상황에서 권위 있는 미국 FDA가 렘데시비르의 긴급사용을 승인했다는 것의 큰 의미를 인지하고 있다"고 말했다.
FDA는 앞서 성명에서 렘데시비르가 호흡 장애로 인공호흡기 등을 필요로 하는 코로나19 중증 입원 환자를 위해 특별히 지정될 것이라고 밝혔다. 트럼프 미국 대통령도 이날 백악관에서 길리어드사(社)의 대니얼 오데이 최고경영자(CEO) 그리고 스티븐 한 FDA 국장과 함께 한 자리에서 긴급승인 을 축하했다. 길리어드사어언스의 오데이 CEO는 이번 FDA 조치가 "중요한 첫걸음"이라며 환자들을 돕기 위해 150만개 분량의 렘데시비르를 기증하고 있다고 전했다. 이는 최소 14만명에게 공급할 수 있는 양DLEK.
FDA의 긴급사용 승인은 연구가 진행 중인 상황에 취할 수 있는 조처로 정식 사용 허가와는 차원이 다르다. 긴급사용 승인으로 처방은 가능하지만 제한된 조건에서 사용할 수 있다.
FDA는 그러면서도 렘데시비르는 간의 염증, 투약과 관련된 문제 등 부작용을 야기할 수 있다고 밝혔다. 메스꺼움과 구토, 식은땀, 저혈압등도 유발할 수 있다고 FDA는 덧붙였다.
김재희 기자 글로벌이노코믹 tiger8280@g-enews.com