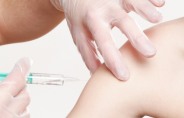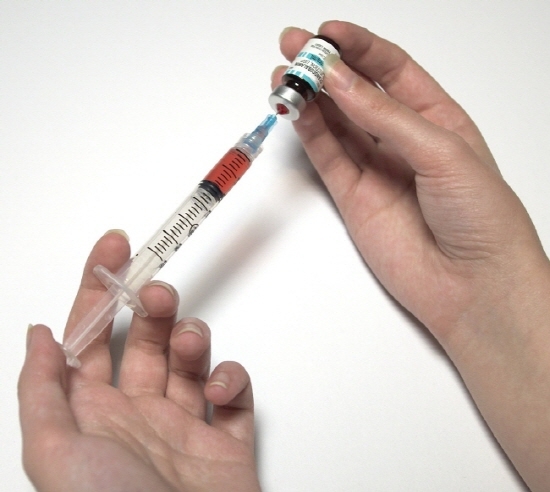
미국 식품의약국(FDA)이 코로나19 백신 긴급승인 기준을 강화한 새로운 지침을 이번 주 발표할 예정이라고 워싱턴포스트(WP)가 22일(현지시간) 보도했다.
매체에 따르면 FDA는 3상 임상시험 참가자가 2차 백신을 투약한 이후 최소 2개월을 추적한 데이터를 제출하도록 할 예정이다.
또한 플라시보(가짜 약) 군과 고령층에서 최소 5명의 중증환자 사례도 찾아내기로 했다.
이 같은 조치는 백신의 안전성과 효능에 대한 국민 신뢰를 높이기 위한 것이다.
여론조사에 따르면 미 국민은 아직 개발되지도 않은 백신에 대해 이미 낮은 기대를 갖고 있다.
트럼프 대통령 등이 백신 개발을 정치적으로 이용하면서 신뢰가 낮아졌기 때문이다.
도널드 트럼프 대통령이 희망한 "대선 전 백신 개발"도 어려울 전망이다.
모더니와 화이자는 7월27일부터 시험을 할 예정이었지만 참가 희망 인원 3만 명의 절반을 모집하는 데에도 약 한 달이 걸렸다.
이 시험은 3, 4주 후 2차 백신을 맞도록 하고 있는데 11월 중순 이전에 이 요건을 충족하는 충분한 자료를 확보하는 것은 사실상 불가능하다는 것이다.
트럼프 대통령은 FDA 내 이른바 '딥 스테이트(숨은 권력집단)'가 자신의 재선을 방해하기 위해 고의로 치료제와 백신 승인을 지연시키고 있다는 음모론을 제기한 바 있다.
이에 대해 스티븐 한 FDA 국장은 "FDA 내에서 딥 스테이트라고 생각되는 사람은 본 적이 없다"며 "FDA 직원들은 미국인의 공익에 집중하고 있다"고 반박한 상태다.
이정선 글로벌이코노믹 기자 bellykim@daum.net