 이미지 확대보기
이미지 확대보기희귀의약품 지정은 희귀난치성 질환의 치료제 개발 및 허가가 원활하게 이루어질 수 있도록 지원하는 제도다. EMA는 유럽에서 인구 1만명 중 5명 이하로 영향을 주는 질병 중 미충족 의료 수요가 높고 환자들에게 상당한 혜택이 예상되는 후보물질을 희귀의약품으로 지정하고 있다.
EMA의 희귀의약품 지정을 받은 후보물질은 △임상시험에 대한 과학적 조언 제공 △허가 수수료 감면 △의약품 허가 시 10년간 독점권 인정 등 혜택이 부여된다.
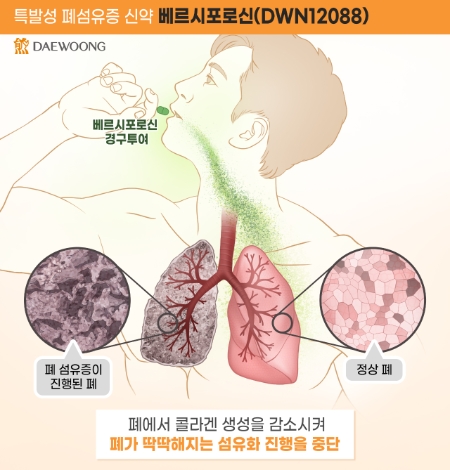
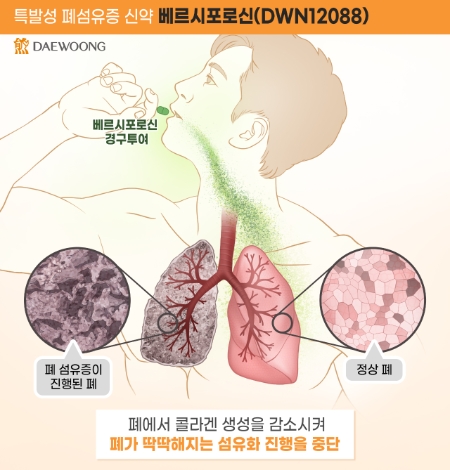
특발성 폐섬유증(IPF)은 폐에 콜라겐이 비정상적으로 축적돼 폐 기능을 상실하는 난치병이다. 세계적으로 인구 10만명 당 13명 정도 발생하며 진단 후 5년 생존율이 40%에 불과할 정도로 예후가 좋지 않은 치명적 질환이지만 기존 치료제는 부작용이 심해 신약 개발이 절실하다.
앞서 베르시포로신은 2022년 미국 식품의약국(FDA)에서 희귀의약품과 패스트트랙 개발 품목으로도 지정됐다. FDA 패스트트랙으로 지정된 약물은 개발 각 단계마다 임상 설계에 대한 상담 및 획득한 자료에 대한 조언 청취 등 허가 승인 과정에서 FDA와 긴밀한 협의가 가능하다. 또한 지난해 12월 국가신약개발사업단(KDDF)의 '신약 임상개발지원' 과제 중 '하이 퍼포먼스' 부문 우수과제로 선정된 바 있다.
전승호 대웅제약 대표는 "대웅제약이 세계 최초로 개발중인 특발성 폐섬유증 신약 베르시포로신은 지난해 중화권 기술수출에 성공하는 등 임상 단계부터 전 세계적인 관심을 받았다"며 "이번 EMA 희귀의약품 지정을 계기로 희귀질환인 특발성 폐섬유증으로 고통 받고 있는 환자들에게 신속하게 치료옵션을 제공할 수 있도록 개발에 더욱 매진하겠다"고 전했다.
이재현 글로벌이코노믹 기자 kiscezyr@g-enews.com