사람의 면역 체계는 몸을 침범하는 바이러스나 다른 병원균과 싸우기 위해 항체를 형성한다. 코로나19의 경우 보호 항체가 얼마나 많이 형성되고 얼마나 오래 지속될지 불분명하지만, 이 테스트는 면역 보호에서 코로나10 항체의 역할을 이해하는 데 도움이 된다고 한다.
FDA는 이 진단기를 승인하면서 인간 내 코로나19 중화 항체의 성격에 대해 많은 부분이 알려지지 않고 있으며 높은 수준의 항체가 반드시 코로나19에 대한 면역성을 보장하지는 않는다고 지적했다. 이 새로운 테스트는 코로나19 항체와 바이러스에 대한 보호 사이의 관계를 더 연구하기 위해 사용될 수 있기 때문에 중요한 의미를 갖는다.
이 테스트는 올해 초 공개된 마운트시나이헬스시스템(Mount Sinai Health System)과 진단 스타트업 리날리틱스(Renalytix)의 합작사인 칸타로 바이오사이언스가 개발했다. 연구개발(R&D) 기업 바이오테크네와의 협력을 통해 현재 월 1000만 건 정도의 테스트를 하고 있다.
마운트시나이의 에릭 리움 책임자는 "이 검사로 면역성 연구와 면역력, 개인이 갖고 있는 항체 수준 간의 관계를 폭넓게 규명하는 것이 가능할 것"이라며 "이미 이 기술이 연구에 활용되고 있다"고 밝혔다. 이 진단의 다음단계 적용은 백신의 사용에서다.
그는 이 검사가 과거 코로나19에 전염돼 이미 높은 수준의 중화 항체를 가진 사람을 알아내는 데 사용될 수 있으며, 이 경우에 해당되는 사람은 백신이 당장 필요하지 않을 것이라고 말했다. 리움 박사는 “한정된 맥신의 투여를 어떻게 배정할지를 결정하는 보건 공무원에게 도움이 될 것이며 코로나19 항체가 없는 사람들에게 집중하는 것이 합리적”이라고 덧붙였다.
리움 박사는 또 이 테스트가 백신의 효과와 그것이 누군가에게서 강력한 면역 반응을 유발하는지 여부를 평가하는 데 사용될 수 있다고 말했다.
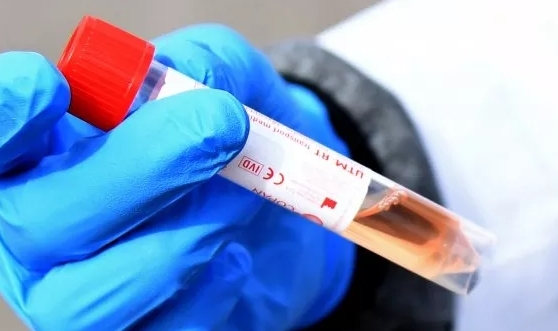
칸타로는 이 테스트는 혈액 샘플을 사용하며 임상 실험실에서 진행되어야 하지만 특별한 별도의 장비가 필요하지 않다고 말했다. 지난 10월 유럽 규제당국으로부터 CE 마크를 받아 유럽연합(EU)에서 사용 중이다.
척 쿠메스 바이오테크네 최고경영자(CEO)는 성명에서 "이번 EUA(비상 사용 허가)를 통해 미국 전역의 임상의들에게 동급 최강의 혈청 검사기를 즉시 공급할 준비가 돼 있다"면서 "우리는 이 코로나19 진단기가 의료 사업자와 정책 입안자의 의사결정에 중요한 역할을 할 것으로 예상하며 추가 수요를 충족시키기 위해 생산을 늘릴 것이다“라고 말했다.
조민성 글로벌이코노믹 기자 mscho@g-enews.com






























![[영상 시승] 전기차 고민이라면? 그냥 아이오닉 5 사~! 2024년형...](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2024042707324903509c35228d2f5175193150103.jpg)
![[뉴욕증시] 알파벳·엔비디아 폭등에 3대 지수 일제히 상승](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2024042705504802175c35228d2f5175193150103.jpg)
























