식약처, 임상 1상 면제하고 2상 승인… 중화항체 농축한 ’고면역글로불린‘ 성분
 이미지 확대보기
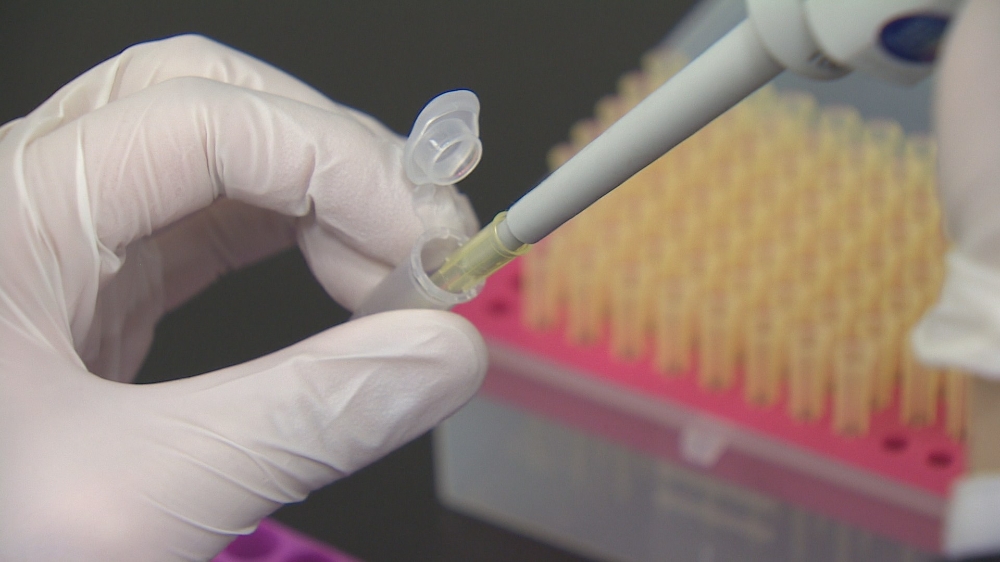
이미지 확대보기식품의약품안전처는 GC녹십자가 신청한 코로나19 혈장치료제 'GC5131' 임상 2상 시험계획(IND)을 승인했다고 20일 밝혔다.
앞서 GC녹십자는 지난달 29일 임상 2상 IND(임상시험계획서)를 식약처에 신청했다고 밝혔다.
이번 임상시험에서는 약물 적정 용량을 설정하고, 안전성과 유효성을 평가하는 것으로 삼성서울병원·서울아산병원·중앙대병원·고대안산병원·충남대병원 등 5개 병원에서 60명을 대상으로 진행할 것으로 알려졌다.
GC녹십자는 이미 지난달 18일 충북 청주시 오창공장에서 ‘GC5131A’의 임상시험용 제품 생산에 들어갔다.
한편 프랑스, 중국, 일본, 이탈리아 등 해외에서도 혈장 치료제를 개발 중이며, 현재 6개의 소규모 임상시험이 진행 중이다.
이태준 글로벌이코노믹 기자 tjlee@g-enews.com