식약처, ICT·바이오·나노 등 첨단기술 보유 의료기기업체 선정 지원나서
 이미지 확대보기
이미지 확대보기1일 관련 업계에 따르면 식품의약품안전처는 올해 '의료기기산업 육성 및 혁신의료기기 지원법' 개정에 따라 혁신의료기기 제도를 본격 가동했다.
혁신의료기기는 정보통신기술, 바이오기술, 나노기술 등 첨단기술을 적용해 기존 의료기기나 치료법보다 안전‧유효성을 개선했거나 개선할 것으로 기대되는 의료기기를 말한다. 관련 규정에 따라 식약처장이 직접 지정하는 것이 특징이다.
혁신의료기기로 지정받는 경우 다른 의료기기에 비해 우선 심사받거나 개발 단계별로 나눠 신속 심사를 받을 수 있는 특례를 받을 수 있다. 이는 허가‧심사의 불확실성을 낮추고 의료기기업체의 허가와 제품화를 지원하기 위한 조치다.
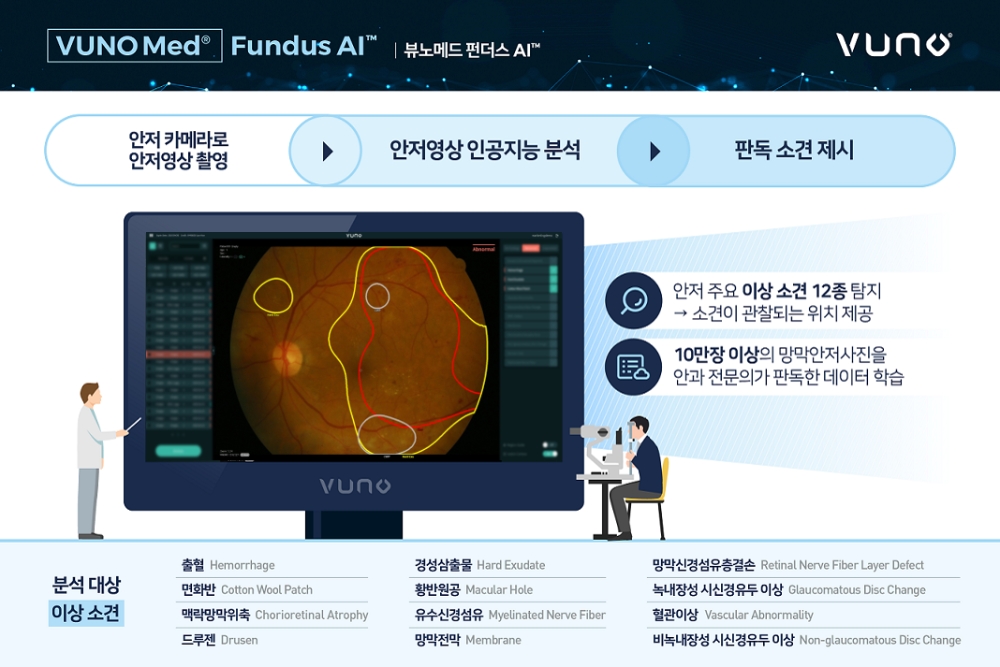
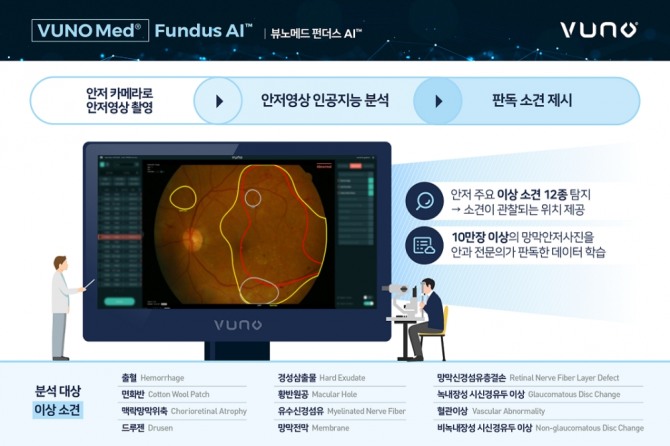
현재까지 총 4개의 의료기기가 혁신의료기기라는 이름을 달았다. 지난 7월과 8월 각각 3건과 1건의 승인이 이뤄졌다. 첫 제품은 ㈜뷰노의 의료영상진단 보조소프트웨어 '뷰노메드 펀더스 AI'다. 이 제품은 인공지능(AI) 기술을 적용해 안저(눈 내부 후면에 해당다는 망막이 있는 부분) 영상을 분석하는 소프트웨어다.
입자가속기로 중성자를 체내에 조사해 암세포를 선택적으로 사멸하는 ㈜다원메닥스의 '치료용중성자 조사장치'와 AI를 활용해 파킨슨병 진단에 도움을 주는 ㈜휴런의 소프트웨어인 'mPDia' 역시 지난 7월 혁신의료기기로 지정받았다.
지난달에는 ㈜스키아의 '마르스-브리스트'가 혁신의료기기로 선정되는 영예를 안았다. 이 제품은 유방 촬영 CT 스캔 영상을 바탕으로 유방 종양의 병변 위치를 증강현실로 보여줘 수술을 보조하는 의료용 네비게이션이라고 할 수 있다.
혁신의료기기 제도 시행으로 의료기기업계의 관심도 높아지고 있다. 4차 산업혁명으로 다양한 IT기술이 의료기기에 적용되고 있는 만큼 신속히 제품을 개발하면 다양한 혜택을 얻을 수 있기 때문이다. 특히 개발 후 제품 출시까지 식약처의 지원을 받을 수 있고 기술력을 인정받아 시장 내 입지를 탄탄히 할 수 있다.
황재용 글로벌이코노믹 기자 hsoul38@g-enews.com