 이미지 확대보기
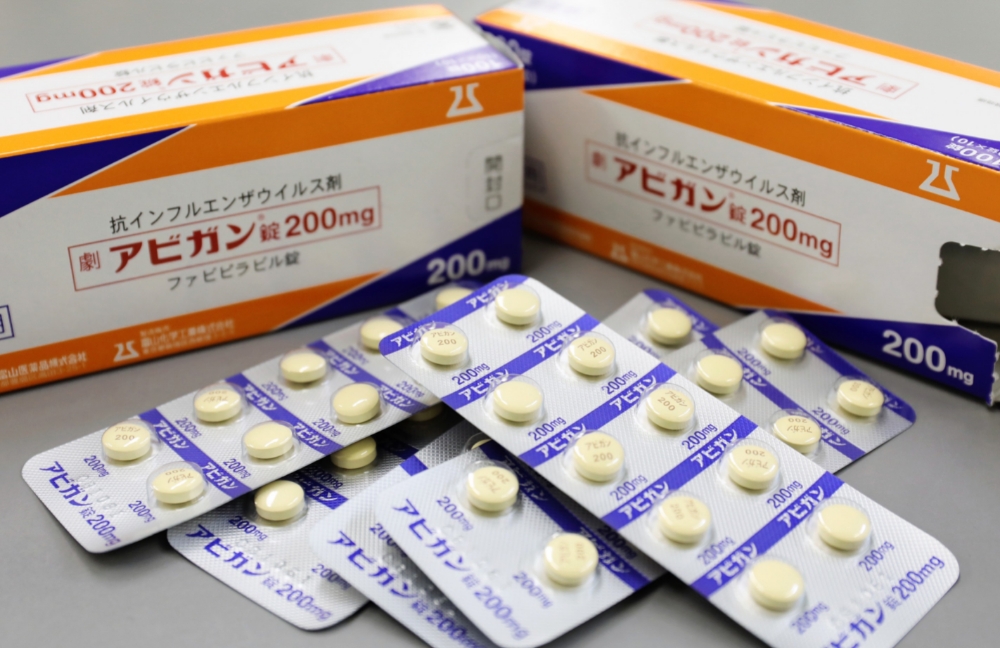
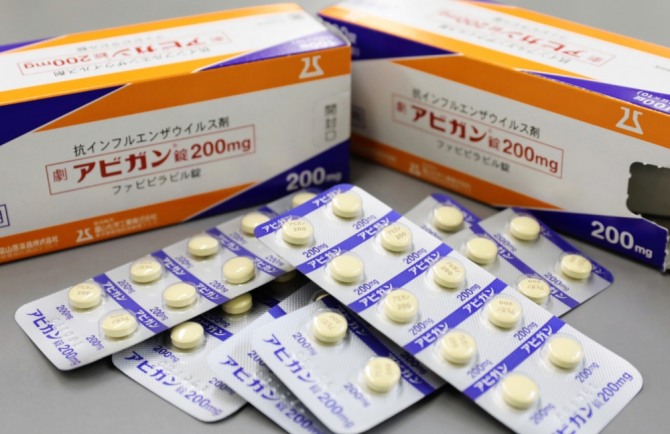
이미지 확대보기아비간은 ‘파빌라비르(Favipiravir)’를 주성분으로 하는 RNA바이러스 치료제이다. 2016년 후지필름의 자회사인 도야마 케미컬(Toyama Chemical)은 아비간 제조 기술을 중국 저장하이정 파마수티컬에 이전했다.
원래 신종 플루 치료제로 개발된 것으로 지난해 일본 정부가 진행한 임상 시험에서 코로나19 환자의 증상 악화를 막고, 무증상자의 발병을 억제 하는 것으로 나타났다.
2020년 2월 중국 국가약품감독관리국(NMPA)은 ‘파빌라비르’를 코로나19 치료제로 허가하고, 제품을 시장에 출시했다.
과거 필름 업계를 대표했던 후지필름홀딩스는 필름 사업을 통해 체득한 화학 기술을 토대로 화장품과 제약, 바이오 기업으로 사업을 확대했다.
최근 후지필름은 의료 분야 투자에 박차를 가하고 있는데, 특허권 상실은 커다란 타격이 될 수 있기 때문이다.
중국 특허 출원에 따르면 중국인민해방군 군사의학연구원(AMMS)은 '코로나바이러스 감염 치료를 위한 파빌라비르 사용' 특허를 받았다.
AMMS는 2020년 1월 21일에 초기 신청서를 제출하고, 같은 해 6월 다시 신청서를 제출했다. 특허는 2021년 3월 29일 심사를 통과했고 이어 5월 4일에 공개됐다.
특허협력조약을 통해 기업과 연구기관은 153개국에서 원 특허일자를 이용해 특허보호 신청을 할 수 있다. AMMS가 실제로 이 표준을 사용했는지 여부는 비공개이다.
중국에서의 승인은 이례적으로 빨랐다. 2019년 중국에서 특허 출원이 허가되기까지 평균 22.5개월이 소요됐다.
한 국제특허변호사는 "신속한 승인은 특허가 가치 있고 우선할 가치가 있다는 것을 보여주는 지표"라고 말했다.
AMMS가 일본에서 정식으로 적용 절차를 시작할 경우, 후지필름이 아비간을 일본에서 코로나바이러스 치료제로 판매할 수 없게 된다.
이 문제에 정통한 사람들에 따르면 후지필름은 보건부에 이 문제를 보고했다. 일반적으로 특허청에 발명품이 새로운 것이 아님을 증명하는 정보를 제공함으로써 특허권을 무효화할 수도 있다.
후지필름 대변인은 중국에서의 특허 승인은 인정했지만 더 이상의 언급은 할 수 없다고 밝혔다.
후지필름은 스마트폰의 부상과 함께 핵심 사업분야인 사진필름 사업이 급속히 쇠퇴하자 지난 2008년 의료분야로 발을 넓히기 위해 도야마 케미컬을 인수했다.
지난 1998년에 처음 개발된 아비간은 바이러스가 세포 안에서 복제되는 것을 막는 효과가 있는 것으로 밝혀졌다. 2014년 일본 후생성은 아비간을 신종 인플루엔자에 대한 응급조치에 한해 조건부 사용 승인을 내렸다.
그러나 일본 보건부는 코로나19 치료제로서는 자료가 불충분 하다는 이유로 승인을 연기했다.
후지필름은 포기하지 않고 4월에 임상시험을 재개했다. 미국과 캐나다에서도 임상 3단계가 진행 중이다.
파빌라비르는 인도와 러시아, 터키 등지에서 긴급 사용 허가를 받았다. 도마야 케이컬의 원래 특허는 대부분의 국가에서 만료되었기 때문에 후지필름은 이 약의 제네릭(generic·복제약)을 생산하는 현지 제약사와 경쟁하고 있다.
유명현 글로벌이코노믹 기자 mhyoo@g-enews.com