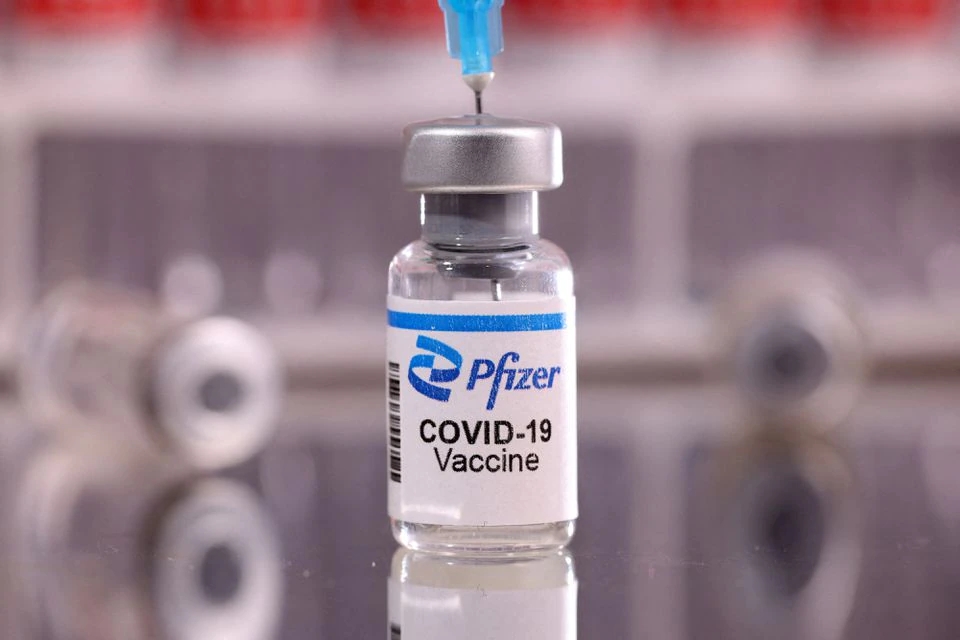
18~55세 1420명 대상 미국과 남아공에서 실시
 이미지 확대보기
이미지 확대보기화이자는 이번 인체 임상시험 대상의 일부 그룹에 속한 사람들이 이미 오미크론 특화 백신을 접종한 상태라고 밝혔다. 이번 임상시험 결과는 올해 상반기에 나올 예정이다.
화이자는 임상시험 결과가 나오기 전에 미국 규제 당국이 허가 절차를 시작하고, 안정성이 확인되면 올해 3월부터 이 백신을 공급하기 시작할 수 있다고 밝혔다. 또 오미크론 특화 백신이 필요하다는 결론이 나면 올해 연말까지 40억 회 분을 생산할 수 있다고 화이자가 밝혔다.
우구르 사힌 바이오엔테크 최고경영자(CEO)는 “이번 연구가 오미크론을 다른 변이와 같은 수준으로 예방하는 동시에 오래 지속되는 백신을 개발하기 위한 학술적 접근”이라고 설명했다.
화이자와 바이오엔테크의 백신 부스터샷이 접종 후 4개월간 오미크론 변이에 강한 보호 효과를 보였다는 연구 결과가 24일 발표됐다. 미 텍사스대 의대와 화이자, 바이오엔테크 연구진들은 백신 접종자의 혈청 샘플 조사와 중화 실험 등을 통해 이런 결과를 얻었다고 밝혔다. 화이자 부스터샷은 오미크론을 중화하는 강도를 증가시켰고, 항체 수준이 시간이 지나면서 다소 감소하지만, 접종 4개월 시점에도 높은 수준의 오미크론 방어 효과가 지속됐다고 연구진이 밝혔다.
화이자와 바이오엔테크는 2주 전 오미크론용 백신 생산을 개시했다고 밝혔었다. 유럽의약품청(EMA)은 아직 오미크론 특화 백신 필요성에 대한 공식적인 견해를 밝히지 않았다. 화이자와 바이오엔테크는 미 정부 당국의 허가받지 않은 상태에서 베타와 델타 변이 특화 백신 개발을 추진했었다.
국기연 글로벌이코노믹 워싱턴 특파원 kuk@g-enews.com