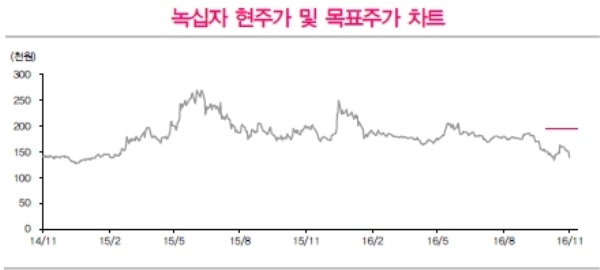
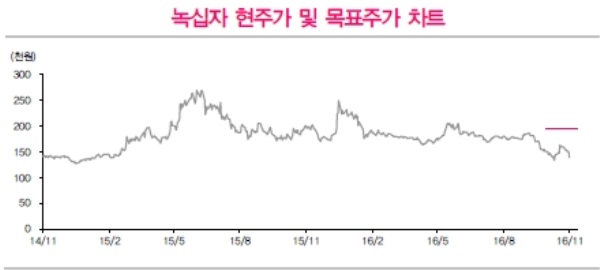
 이미지 확대보기
이미지 확대보기미국식품의약국(FDA)가 15년11월 허가 신청한 혈액제제 IVIGSN에 대해 검토완료공문(CRL, Complete Response Letter)을 통해 제조공정 관련 보완자료를 요청했다.
회사 측은 제품의 유효성 및 안전성에 대한 문제 제기는 없었다고 설명했으며,보완자료를 준비를 위한 오창A공장의 시험생산과 재승인 신청 일정을 조율중인 것으로 밝혔다.
아시아 기업으로는 첫 시도였던 혈액제제 FDA 승인이 1차 시도에서 불발 되었으나, 최종 승인을 위한 구체적 조건을 확인할 수 있는 사실은 기회다.
출시지연에 따른 타격도 제한적이라는 분석이다. 출시가 지연되었으나 기존 17년 추정치에서 혈액제제의 미국 수출 비중은 낮다.
16년 6월 FDA 실사 완료한 오창A공장은 65만리터, IVIG혈액제제 기준 600억원 규모의 생산이 가능하며 3Q16기준 67%의 평균 가동률을 보이고 있는데, 본격적인 미국 수출은 19년에 가동되는 캐나다 공장(100만리터)의 비중이 더 높다는 지적이다.
구자용 동부증권 연구원은 "17년 매출추정치를 일부 하향 조정할 수 있을 수 있으나, 허가가 완전 무산될 위험요인이 아니기 때문에 장기적 성장성은 유효하다"라며 "최근 주가 흐름에 해당 섹터의 높은 변동성이 반영되고 있으나 녹십자의 투자 매력은 여전히 높다고 판단한다
최성해 기자 bada@
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.