지난달 10일 식약처 임상 3상 시험계획 승인…내년 상용화 목표
냉장 보관 가능해 저개발국 접근성 확보, 국내 백신 수급에도 도움
"GBP510 플랫폼 토대 변이 바이러스 대응 능력 키울 수 있을 것"
냉장 보관 가능해 저개발국 접근성 확보, 국내 백신 수급에도 도움
"GBP510 플랫폼 토대 변이 바이러스 대응 능력 키울 수 있을 것"
 이미지 확대보기
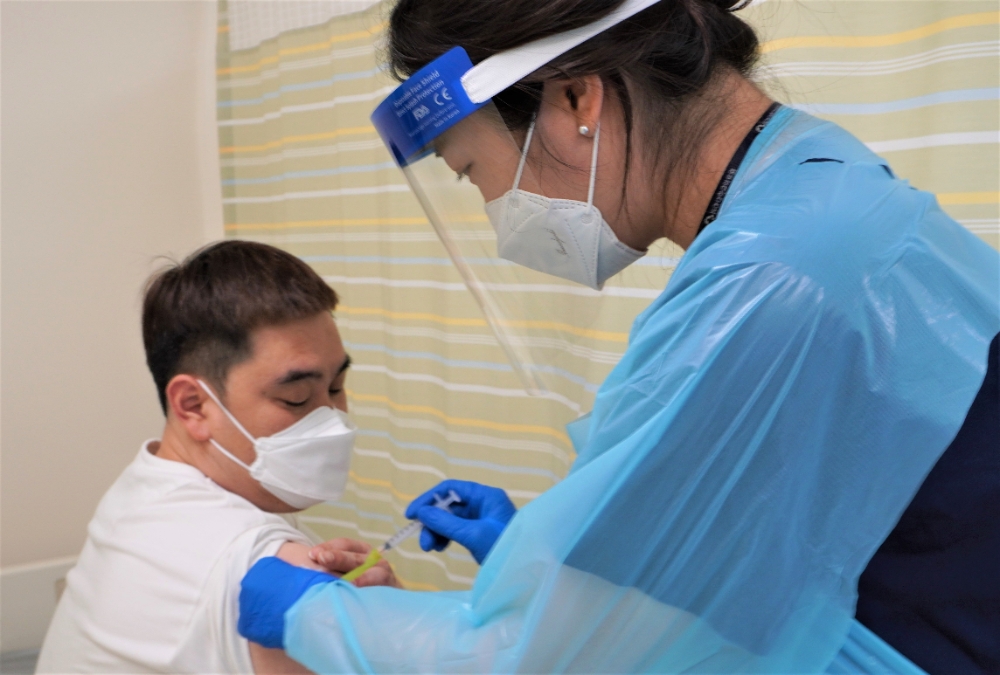
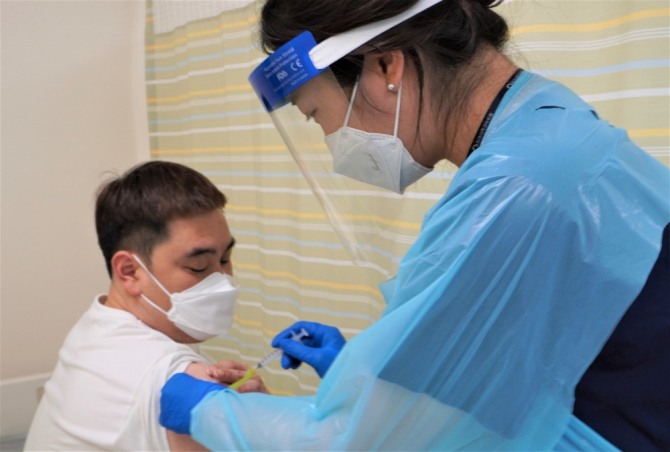
이미지 확대보기지난달 31일 업계에 따르면 SK바이오사이언스는 미국 워싱턴대학 항원디자인연구소(IPD)와 공동 개발한 코로나19 백신 후보물질 GBP510의 임상 3상 시험 첫 피험자 투여를 개시했다.
지난달 10일 식품의약품안전처가 GBP510 임상 3상 시험계획을 승인한 지 약 3주 만이다. 회사는 앞서 지난 6월 28일 임상 3상을 신청했고 식약처는 검토를 거쳐 40여 일 만에 승인 결정을 내렸다.
 이미지 확대보기
이미지 확대보기◇ 국내외 기관에서 성인 4000여 명 대상 임상 3상 본격화
SK바이오사이언스는 비영리 국제기구인 국제백신연구소(IVI)와 손잡고 동유럽, 동남아 등 해외에서도 각 국가별 임상 3상 시험계획 승인을 신청 중으로 빠르면 내달부터 임상에 돌입한다는 계획이다.
회사는 내년 1분기 3상 임상에 대한 중간 분석 결과가 나온 뒤 정식 허가를 신청할 계획이며 전문가들은 이르면 내년 상반기경 상용화가 가능할 것으로 내다보고 있다.
SK바이오사이언스의 임상 3상 돌입은 '백신 주권' 확보를 위한 시작점이라는 데 큰 의미가 있다. 김강립 식약처장은 임상 3상 승인 당시 “국산 백신이 최초로 3상에 돌입함에 따라 국내 백신 자급화를 위한 첫걸음을 내디뎠다는데 의의가 있다”고 강조했다.
문재인 대통령 또한 "국산 1호 백신이 탄생해 상용화될 수 있기를 기대한다"면서 “국내 임상 시험이 신속하게 충분히 이뤄질 수 있도록 정부는 전방위로 지원할 것”이라고 약속했다.
 이미지 확대보기
이미지 확대보기◇ 2~8도 냉장 보관 가능…저개발국도 접근성 확보
SK바이오사이언스의 백신 후보물질은 유전자 재조합 기술을 이용한다. 코로나19 바이러스의 표면항원 단백질을 인체에 주입해 중화항체(특정 바이러스를 중화할 수 있는 항체) 생성을 유도하는 방식으로 노바백스의 코로나19 백신과 동일한 기술이다.
모더나, 화이자 등은 메신저 리보핵산(mRNA) 백신인데 이는 바이러스의 항원 유전자를 mRNA 형태로 주입, 체내에서 항원 단백질을 생성해 면역반응을 유도한다. 안전성이 높고 저비용 대량생산이 가능하지만 온도·화학물질 등 외부 환경에 취약하다는 단점이 있다.
SK바이오사이언스 관계자는 "GBP510에 적용된 합성항원 백신 플랫폼은 2∼8도의 냉장 조건에서 보관이 가능해 기존 백신 물류망을 활용해 유통할 수 있다"면서 "장기보관도 가능해 저개발국에서도 접근성을 확보할 수 있을 것으로 보인다"고 강조했다.
또한 "수입에 의존하고 있는 국내 코로나19 백신 수급 상황에도 숨통이 트일 것"이라며 "SK바이오사이언스의 기술로 개발된 국산 백신인만큼 생산·공급 계획을 자체 수립할 수 있다"고 설명했다.
◇ 코백스 퍼실리티 우선 공급, 변이 대응 등 우려도 나와
다만 일각에서는 SK바이오사이언스 백신의 국내 우선 배정이 불투명하다는 우려가 나온다. GBP510 개발 초기 단계부터 빌&멜린다게이츠재단과 CEPI(전염병대비혁신연합)에서 총 2억 1370만 달러(약 2450억 원)의 자금을 지원받았기 때문이다.
CEPI 자금을 지원받으면 약 180개국이 참여하는 '코백스 퍼실리티'에 백신을 우선 공급해야 한다. 이와 관련 SK바이오사이언스 관계자는 "국내 배정 물량이 충분할 것으로 보고 있다"고 말했다.
또 GBP510이 오리지널 코로나 바이러스를 겨냥한 백신인 만큼 델타 변이 등 변이 바이러스 상황을 지켜봐야 한다는 지적도 제기된다. 회사는 변이 바이러스 대응 연구도 동시 진행 중으로 알려졌다.
SK바이오사이언스 관계자는 "임상을 통해 변이 바이러스에 대한 예방효과도 확인할 예정"이라며 "장기적으로는 GBP510 플랫폼을 토대로 변이 바이러스 대응 능력도 키울 수 있을 것"이라고 설명했다.
이하린 글로벌이코노믹 기자 may@g-enews.com