 이미지 확대보기
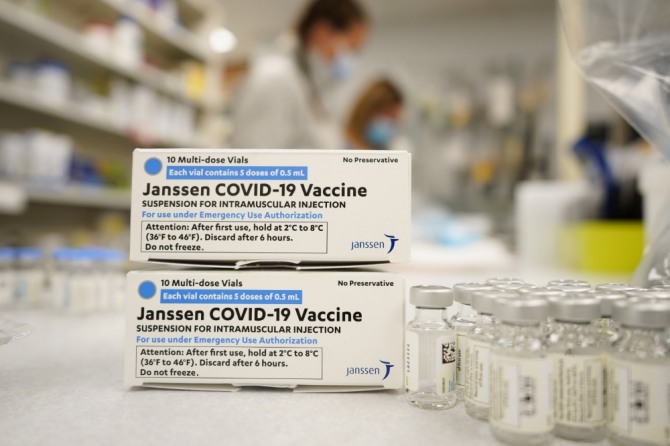
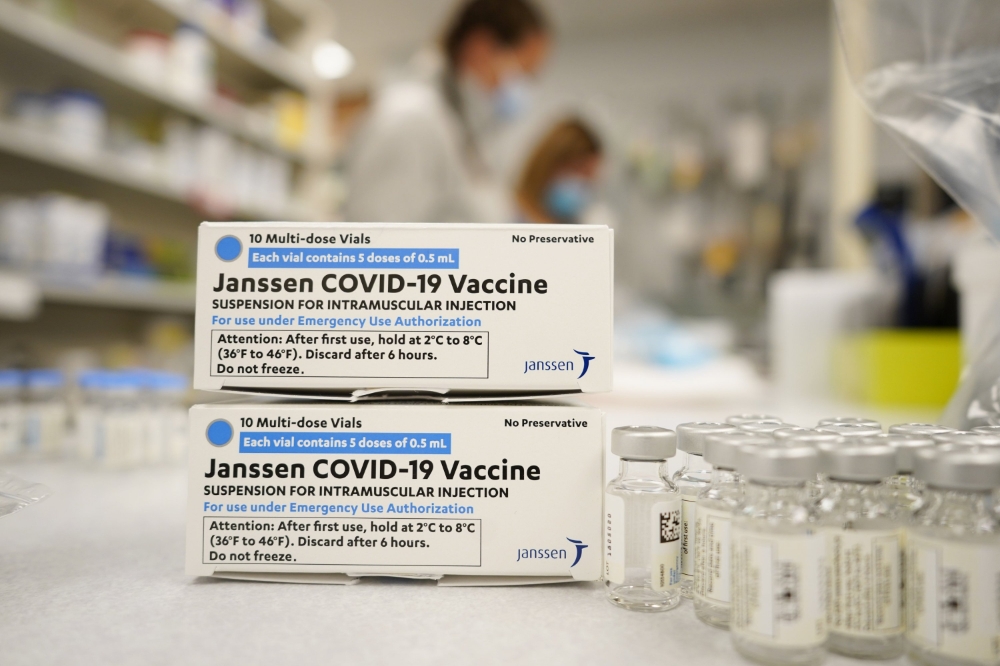
이미지 확대보기FDA는 성명을 통해 얀센 코로나19 백신 접종 후 혈소판감소증후군(TTS)을 동반한 혈전증이라는 희귀하고 위험한 질환 때문이라고 밝혔다.
FDA는 얀센 코로나19 백신의 접종을 해도 되는 대상을 다음과 같이 제한했다.
- 화이자/모더나 백신과 같은 mRNA 백신에 심각한 알레르기 반응을 보인 사람
- mRNA 백신에 대해 개인적인 우려를 가진 사람들
미국 질병통제예방센터(CDC)에 따르면 5일 현재 미국에서 1870만 회분 이상의 얀센 코로나19 백신이 투여됐다. 백신 접종 완료자로 간주되는 사람들 중 7.7%가 이 백신을 맞았다.
CDC 백신자문위원회는 TTS에 대한 동일한 우려를 언급했다.
CDC와 FDA는 이전에 TTS에 대한 보고에 대해 얀센 코로나19 백신 사용을 중단할 것을 권고한 바 있다.
존슨앤드존슨은 당시 성명을 통해 "우리 제품을 사용하는 사람들의 안전과 복지가 우리의 최우선 과제다. 얀센 코로나19 백신을 접종한 소수의 사람들 중 혈소판 감소증과 함께 혈전증 발생이라는 매우 드문 질병을 앓고 있다. 우리는 의료 전문가 및 보건 당국과 긴밀히 협력하고 있으며, 의료 전문가 및 대중들에게 이 정보를 공개하는 것을 강력히 지지한다"고 밝혔다.
FDA는 백신 유해 현상 보고 시스템(VAERS)에 근거, 지난 3월 18일까지 9명의 사망자를 포함하여 60명의 TTS 사례를 확인했다고 밝혔다.
전반적으로, TTS의 위험은 매우 드문데, TTS의 가장 높은 발생 비율을 보인 층은 30~49세 여성이다. 이 연령대의 여성에게는 100만 회분 당 약 8건의 백신이 투여되었다.
TTS의 경우는 일반적으로 백신 접종 후 1~2주 후에 시작한다. 증상으로는 호흡 곤란, 흉통, 다리 붓기, 지속적인 복통, 두통이나 시야 흐림과 같은 신경학적 증상, 백신 접종 부위 너머 페티키아라고 불리는 피부 바로 아래에 생기는 붉은 반점이 있다.
정대민 글로벌이코노믹 기자 dmjeong@g-enews.com























![[특징주] 현대차, 새만금 9조 투자 소식에 10% 급등 '훨훨'](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2026022716542504293edf69f862c617739124.jpg)














