이미지 확대보기
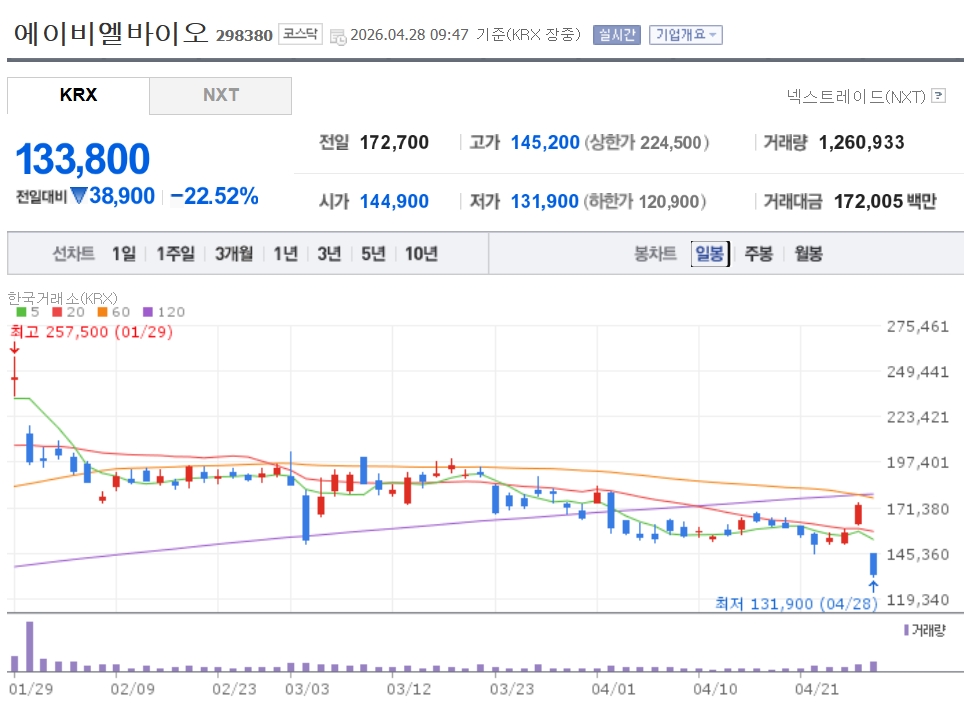
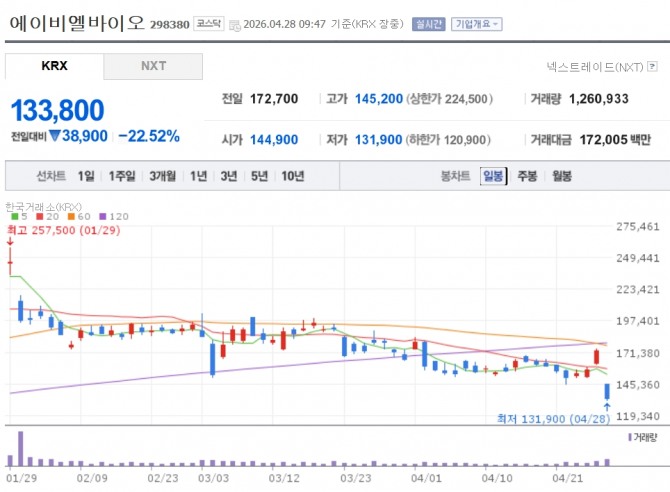
이미지 확대보기28일 한국거래소에 따르면 28일 오전 9시47분 기준 에이비엘바이오는 전일 대비 22.52% 내린 13만3800원에 거래되고 있다.
 이미지 확대보기
이미지 확대보기전날 밤 미국 자회사 컴퍼스테라퓨틱스가 담도암 치료제 토베시미그(ABL001)의 임상 2·3상 최종 데이터를 발표한 것이 악재로 작용했다. 이날 결과 발표 이후 컴퍼스 테라퓨틱스 주가(나스닥)는 전 거래일 대비 64.3% 폭락한 1.79달러에 장을 마감했다.
이번에 추가로 공개된 무진행생존기간(PFS) 중앙값 역시 토베시미그 병용군이 4.7개월을 기록, 대조군(2.6개월) 대비 질병 진행 위험을 56% 낮췄다. 1차 및 2차 지표인 ORR과 PFS라는 핵심 지표에서 유의미한 결과를 도출했다.
하지만 또 다른 주요 평가지표인 전체생존기간(OS)은 통계적 유의성 기준을 충족하지 못했다. 토베시미그 투여군의 OS 중앙값은 9.5개월로 대조군의 7.9개월 대비 수치상 개선은 확인됐으나 통계적 유의성은 확보하지 못했다.
미 식품의약국(FDA) 허가도 쉽지 않을 것이란 전망이 나온다. 김민정 DS투자증권 연구원은 “FDA는 임상 2·3상에서 최종 mOS 데이터를 요구했는데, 통계적 우월성 달성에 실패했기에 허가 획득은 쉽지 않을 것”이라고 밝혔다.
다만 ABL001의 상업성 자체는 본래 제한적이었다는 평가도 나온다. 김 연구원은 “담도암 환자 수가 매우 적고 투약 기간도 짧아 상업성이 미미했다”며 “에이비엘바이오의 기업가치 핵심은 BBB 셔틀 플랫폼(Grabody B)과 ABL111로 인체 개념검증(PoC)이 입증된 Grabody T 플랫폼”이라고 설명했다.
김은진 글로벌이코노믹 기자 happyny777@g-enews.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.