 이미지 확대보기
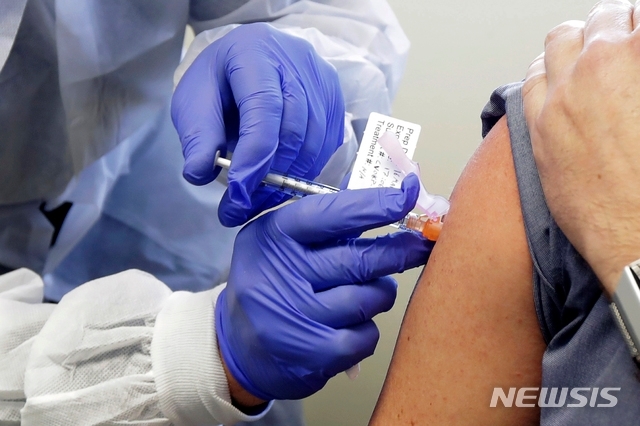
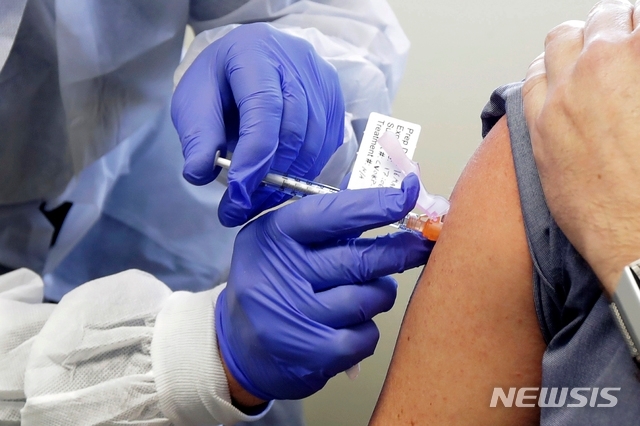
이미지 확대보기공동성명 초안은 백신 접종자의 안전을 최우선으로 할 것을 약속한다는 내용이 골자다. 이번 약속에는 화이자, 존슨앤드존슨, 모더나, 사노피 등이 참여할 것으로 보인다.
이번 공약은 과학자들과 공중보건 전문가들이 트럼프 행정부가 11월 대선 전에 백신을 허가하도록 감독당국, 특히 식품의약국(FDA)에 압력을 행사하고 있다고 우려를 표명하는 가운데 나온 것이다.
월스트리트저널에 따르면 성명 초안은 "우리는 이 서약이 궁극적으로 승인될 수 있는 코로나19 백신에 대한 대중의 신뢰를 보장하고, 그들이 평가받는 엄격한 과학 및 규제 과정을 준수하는 데 도움이 될 것으로 믿는다"는 내용이다.
FDA는 지난 3월 코로나19 환자를 치료하는 데 트럼프가 지원하는 말라리아 치료제 클로로킨과 히드록시클로로킨을 사용할 수 있도록 긴급 허가를 내줬다. 그러나 FDA는 지난 6월, 이 약이 심장 합병증을 유발하고 일부 코로나19 환자의 사망 위험을 증가시킬 수 있다는 새로운 증거에 근거해 허가를 취소했다.
규제당국과 제약회사들은 전 세계 2660만 명 이상의 감염자와 87만 5400명의 사망자를 낸 코로나19를 효과적으로 안전하게 예방하는 백신을 시장에 출시하기 위해 기록적인 속도로 움직이고 있다. 예보관들과 역학자들이 오는 겨울이 더 치명적일 수 있다고 경고하고 있기 때문에 위험 부담이 크다.
미국은 코로나19 백신과 치료제를 신속하게 배포하기 위한 트럼프 행정부의 정책을 통해 6가지 다른 백신 후보에 100억 달러 이상을 투자했다. 모더나, 화이자, 아스트라제네카 등 3개 업체는 이미 3단계 시험을 진행하고 있다. 아스트라제네카의 공동 선언 참여 여부는 불투명하지만 앞서 회사는 '과학을 따른다', '환자가 우선이다'는 내용의 성명을 발표한 바 있다.
민주당 해리스 부통령 후보는 CNN방송과의 인터뷰에서 "트럼프 대통령이 선거 캠페인의 일환으로 백신을 활용할 수 있다"고 우려했다. 그녀는 "60일도 안 남은 선거에서 트럼프 자신이 이 문제에 대해 리더가 될 수 있는 것처럼 행동할 수 있다"고 말했다. 이어 "백신의 안전성과 효능은 공공데이터와 외부 평가만으로 확신할 수 있을 것"이라고 덧붙였다.
조민성 글로벌이코노믹 기자 mscho@g-enews.com