성인 백신 용량의 10분의 1로 줄여 2월 말부터 2회 접종 추진
 이미지 확대보기
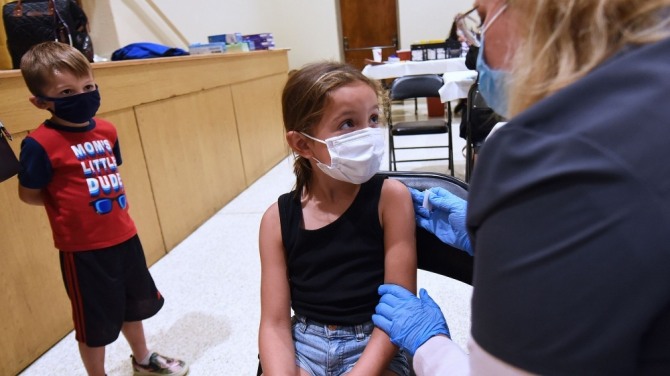
이미지 확대보기화이자 백신은 연령대에 따라 세 종류로 구분된다. 우선 12세 이상과 성인을 대상으로 한 백신이 있고, 이 백신의 용량을 3분의 1로 줄여 5~11세 연령층을 대상으로 백신 접종을 한다. 화이자는 생후 6개월~4세 연령층을 대상으로 성인용 백신의 10분 1 용량만을 사용한다.
화이자는 생후 6개월~4세 아동에게는 백신 용량을 줄이는 대신에 3회 접종이 필요할 수도 있다고 설명했다. 어린 아동에게 백신 접종을 했을 때 쉽게 항체가 형성되지 않을 수 있어 3회 접종의 효능을 시험하고 있다고 화이자가 밝혔다. 그러나 화이자는 이번에 아동에게도 2회 접종을 기준으로 사용 승인 신청을 한다.
화이자는 일단 2회 접종을 추진하고, 3회 접종 효능에 관한 결과가 나오면 추가 접종 여부를 확정하면 된다고 밝혔다.
화이자가 지난해 12월에 2∼4세 아동에게 성인 백신 용량의 10분의 1을 투약한 결과 16~25세 연령층에 백신을 접종했을 때와 비교할 때 안전 문제가 제기되지는 않았으나 효능이 약간 떨어지는 것으로 나타났다. 화이자는 그 이후 이들 아동에게 3회 접종을 한 뒤 그 결과를 기다리고 있다.
국기연 글로벌이코노믹 워싱턴 특파원 kuk@g-enews.com




























![[초점] 화웨이, 1인치 카메라 센서 자체 개발... 스마트폰 시장 ...](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2025051108175409234fbbec65dfb1161228193.jpg)












